Det vides, at alle stoffer er sammensat af molekyler. Men hvad er molekylerne selv lavet af? Lad os se nærmere på dette spørgsmål.
Hvad er et molekyle?
Navnet "molekyle" stammer fra den latinske molekyle - det er en formindskelse af ordet mol (masse oversat). Deres eksistens blev først bevist i et eksperiment i 1906 af J. Perrin, en fransk fysiker, da han studerede Brownsk bevægelse.

I kemi er dette navnet på en separat partikel af stof, der består af 2 eller flere atomer, der er forbundet sammen med kovalente bindinger. Kvantemekanik definerer det som et system, der ikke består af atomer, men af deres kerner og elektroner, der interagerer med dem.
Interessant fakta: Fysik kalder molekyler ikke kun polyatomiske partikler, men også monatomiske, der består af atomer, der ikke er forbundet med kemiske bindinger (ren kviksølv eller inerte gasser). I dette tilfælde kombineres begreberne "molekyle" og "atom".
Normalt er molekylerne elektrisk neutrale, da antallet af protoner og elektroner i dem er det samme, men der er molekyler, der har en elektrisk ladning (de kaldes ioner).
Partikler af et stof med høj molekylvægt kaldes makromolekyler. De består af proteiner, nukleinsyrer, enzymer, polysaccharider, aminosyrer, komplekse lipider og individuelle kunstigt oprettede forbindelser, for eksempel polymerer. De inkluderer hundreder og tusinder af atomer. Derivater af kulbrinter - organiske stoffer og biopolymerer har som regel ikke kun en stor masse, men er også mere komplekse end uorganiske forbindelser.
Molekylær struktur
Molekylerne i en hvilken som helst forbindelse har den samme sammensætning, det har altid det samme antal atomer, kemiske egenskaber afhænger af de valensbindinger, der holder dem sammen. Den klassiske teori betragter molekylet som en dynamisk struktur bestående af atomkerner og deres grupper og et vist antal elektroner placeret på interne og eksterne niveauer.
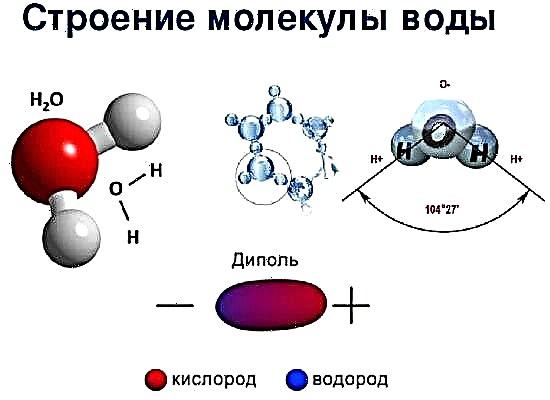
Kemiske bindinger danner normalt kun eksterne elektroner. En binding dannes af 1,2 eller 3 par elektroner med 2 tilstødende atomer (som et resultat, hvori en elektronsky vises). Atomernes interaktionsenergi afhænger af afstanden, hvorpå de befinder sig, og bidrager til molekylets stabilitet under almindelige forhold: det tillader ikke atomer at komme for tæt på hinanden.
Atomer kan oplades positivt og negativt, deres antal er altid konstant. Strukturen og sammensætningen af molekylerne i et bestemt stof påvirkes ikke af den måde, det blev opnået, dvs. et kunstigt produceret stof vil være nøjagtigt det samme som naturligt.
Den molekylære sammensætning skrives ved hjælp af kemiske formler. Strukturen bestemmer, hvilke fysiske egenskaber et stof vil have.
Interessant fakta: organisk stof, vand, kuldioxid smelter og kog ved relativt lave temperaturer og bevarer deres struktur i fast tilstand. Mange uorganiske stoffer består ikke af molekyler, men af atomer (krystaller, rene metaller osv.).
Molekyler i videnskab
I kemi er dette det grundlæggende koncept, molekylstrukturen bestemmes på grundlag af kemiske reaktioner med et stof.Det er også muligt, at kende strukturen, at bestemme, hvad reaktionerne vil være. Som et resultat af kemiske studier blev størstedelen af viden om molekylær funktionalitet og struktur opnået.
Strukturen i fysik forklarer de fysiske egenskaber ved væsker, gasser og faste stoffer. Mobiliteten af molekylerne bestemmer, hvor hurtigt et stof er i stand til at trænge ind i et andet ved kontakt, niveauet for viskositet og den termiske ledningsevne.
I biologien er molekylære egenskaber og den rumlige struktur af største betydning, da alle levende ting fungerer på grund af den delikate balance i samspillet mellem molekyler (kemisk og ikke-kemisk).
Spørgsmålet om, hvad molekyler består af, kan besvares på denne måde - fra et vist antal atomer forbundet med kemiske bindinger. Alle stoffer på planeten består af molekyler.hvis fysiske og kemiske egenskaber bestemmes af molekylernes struktur og sammensætning.